Действительно ли загрязнение эндоскопов представляет серьезную проблему?
Согласно имеющимся данным, с загрязненными эндоскопами связано больше случаев внутрибольничной инфекции или вспышек псевдоинфекции, чем с любыми другими медицинскими устройствами1.
Результаты исследования, проведенного комитетом Сената США, свидетельствуют о том, что в период с 2012 года по весну 2015 года в мире зафиксировано по меньшей мере 250 случаев жизнеугрожающих инфекций, связанных с использованием эндоскопов, включая инфицирование супербактериями семейства Enterobacteriaceae, обладающими резистентностью к карбапенемам2.
ECRI, некоммерческая организация из США, специализирующаяся на повышении безопасности для пациентов, включила загрязнение и недостаточную дезинфекцию эндоскопов в список наиболее серьезных угроз, которым подвергаются пациенты. По этой причине ECRI последовательно включала эту угрозу в свой ежегодно публикуемый список «10 наибольших технологических опасностей для здоровья» на протяжении 9 последних лет3.
Опасность биопленки на многоразовых эндоскопах
Обычные процедуры обработки не позволяют гарантированно избавиться от биопленки, образующейся в каналах эндоскопа21.
Для того чтобы определить начальную стадию колонизации и образования биопленки в эндоскопе, а также предотвратить контаминацию и инфицирование пациентов в ходе эндоскопических процедур, необходимо осуществлять микробиологический контроль при повторной обработке эндоскопа22.
FDA требует осуществлять инфекционный контроль
12 марта 2015 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) объявило о новых мерах, направленных на повышение безопасности многоразовых медицинских устройств и борьбу с возможным распространением инфекционных агентов при многократном использовании таких устройств4, 5, 6.
Информационное письмо FDA о безопасности бронхоскопов
С тех пор FDA опубликовало новые руководящие указания о повторной обработке медицинских устройств, организовало двухдневный семинар, посвященный передаче инфекции при проведении эндоскопических процедур, вынесло производителям дуоденоскопов предупреждение о недопустимости игнорирования требования о представлении отчетности о медицинском оборудовании (MDR), а также выпустило информационное письмо об инфекциях, передающихся через подвергнутые повторной обработке гибкие бронхоскопы6.
Мероприятия FDA
Март 2015 г.:
Новые руководящие указания о повторной обработке медицинских устройств.
Май 2015 г.:
Двухдневный семинар, посвященный проблемам, связанным с контаминированными эндоскопами.
Август 2015 г.:
Требование о проведении исследований, посвященных послепродажному контролю за состоянием эндоскопов.
Август 2015 г.:
Вынесение предупреждения производителям дуоденоскопов.
Сентябрь 2015 г.:
Информационное письмо о безопасности бронхоскопов.
Ноябрь 2016 г.:
Регистрация факта смерти двух пациентов в одном из медучреждений США в результате контаминирования бронхоскопов7.
Январь 2017 г.:
Побит рекорд по отчетам MDR о контаминированных бронхоскопах: в 2016 г. в адрес FDA было направлено 183 соответствующих отчета.
Январь 2018 г.:
Установлен новый рекорд: в 2017 г. в адрес FDA было направлено 215 отчетов MDR о контаминированных бронхоскопах.
Март 2018 г.:
Производителям дуоденоскопов вынесено предупреждение о несоблюдении ими требования о проведении послепродажных исследований, посвященных оценке контаминационных рисков.
Систематический рост несоблюдения стандарта инфекционного контроля, направленного на снижение инфекционных рисков
Несоблюдение в госпиталях США стандарта IC.02.02.01
НКО Joint Commission («Объединенная комиссия») осуществляет аккредитацию и сертификацию примерно 21 000 организаций и программ в сфере здравоохранения США.
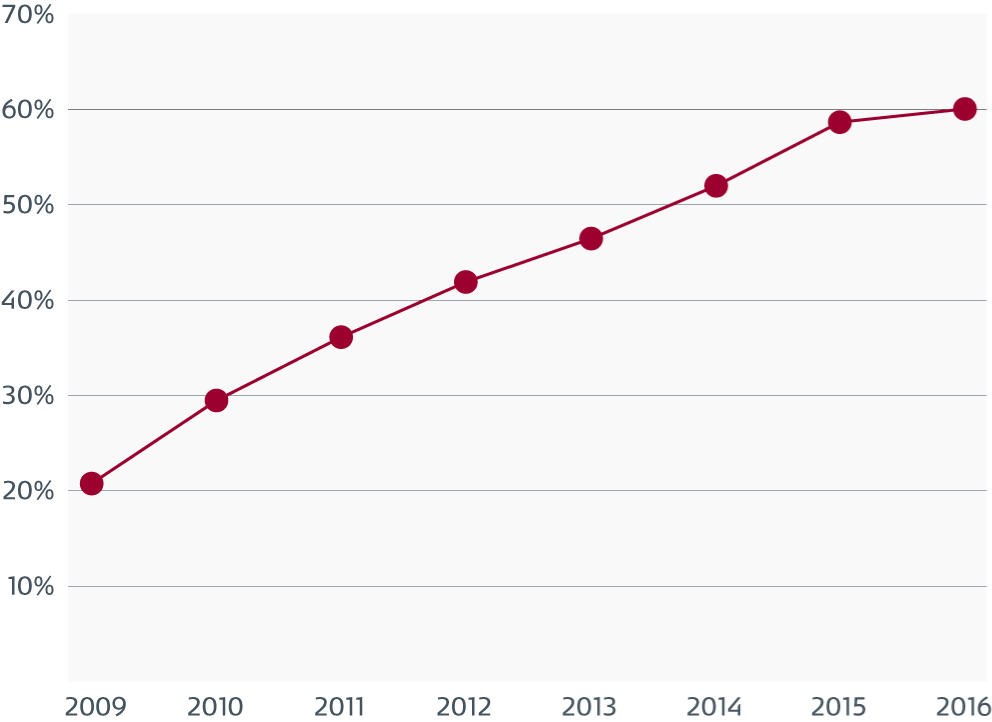
Стандарт Joint Commission IC.02.02.01 предписывает организациям работать над сокращением инфекционных рисков, связанных с медицинским оборудованием, устройствами и расходными материалами. С 2009 года отмечается систематический рост несоблюдения стандарта IC.02.02.01, связанный с недостаточным уровнем дезинфекции и стерилизации оборудования.
«Согласно данным, которыми располагает Joint Commission на текущий момент, количество деклараций о непосредственной угрозе жизни, напрямую связанной с несоблюдением необходимого уровня дезинфекции и стерилизации оборудования, за период с 2013 по 2016 гг. существенно возросло. В 2016 году количество всех случаев непосредственной угрозы жизни, связанных с недостаточной дезинфекцией или стерилизацией оборудования, составляло 74 %»23.
Инфицированные бронхоскопы представляют особую опасность
Гибкие бронхоскопы с трудом поддаются очистке и дезинфекции, в связи с наличием в их конструкции длинных и тонких рабочих каналов и деликатных материалов. Вопрос заключается в том, можно ли гарантировать 100-процентную дезинфекцию каждого бронхоскопа. Несмотря на соблюдение инструкций по обработке, систематически отмечается остаточное загрязнение устройств. При этом даже незначительное отклонение от инструкций по обработке может привести к наличию инфекции в бронхоскопе6, 8.
Обычной обработки недостаточно
Судя по всему, истинный масштаб перекрестной контаминации и инфицирования в ходе выполнения процедур с использованием гибких бронхоскопов остается недооцененным по причине сокрытия части подобных случаев, а также отсутствия или недостаточности контроля8, 9.
В опубликованном в 2013 году обзоре, посвященном инфекциям, связанным с использованием гибких бронхоскопов, проанализировано 50 исследований. При этом в 30 из них сообщается об обнаружении у пациента того же контаминанта, что и на бронхоскопе. В общей сложности 569 случаев контаминирования и 115 случаев инфицирования пациентов (20,21 %) могут быть напрямую связаны с загрязненными бронхоскопами8.
Обычная обработка не обеспечивает эффективного удаления биопленки из каналов эндоскопа. Несмотря на то что в описываемом примере в 12 из 13 эндоскопов была проведена надлежащая обработка каналов, биопленка была обнаружена во всех устройствах10.
В другом исследовании рост микроорганизмов был обнаружен в 32 из 45 эндоскопов (71 %)17.
Загрязнение и микроорганизмы в аспирационных каналах
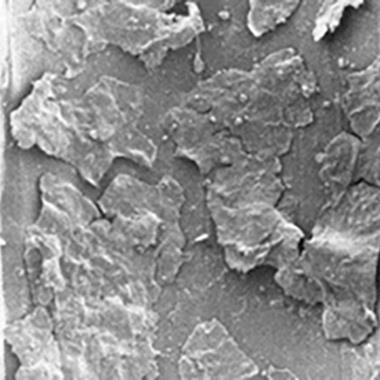
Поверхностные дефекты на снимке, полученном с помощью электронного микроскопа.
Биологическое загрязнение связано с наличием дефектов поверхности, однако может образовываться и на неповрежденных областях.

Увеличенное изображение одной из дефектных областей, на котором видны загрязнения и различные типы микроорганизмов.
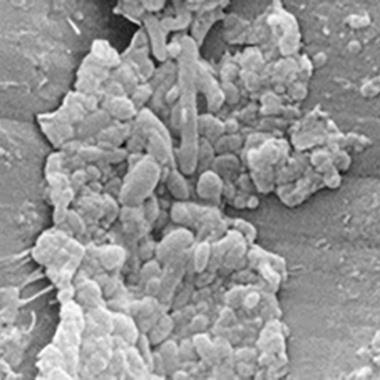
Загрязнения и биопленка в воздушных или водяных каналах
Электронные микрофотоснимки с изображением биопленки на двух различных каналах для подачи воздуха/воды.
Снимок с небольшим увеличением, на котором показан непрерывный слой загрязнения и биопленки.
Многослойная биопленка, состоящая из здоровых на вид клеток, окруженных и перекрываемых аморфными на вид экзополисахаридами.

Риски, связанные с резистентными штаммами бактерий, увеличиваются
Реаниматологам, медработникам, занимающимся уходом за больными, и другим сотрудникам системы здравоохранения, имеющим отношение к инфекционному контролю, давно известно о рисках контаминирования и инфицирования пациентов в ходе медицинских манипуляций. Появление микроорганизмов с множественной медикаментозной устойчивостью, таких как энтеробактерии, обладающие резистентностью к карбапенемам, или мультирезистентная синегнойная палочка, несет с собой новые риски для пациентов, врачей, госпиталей и клиник.
Сообщается о вспышках инфекций, связанных с использованием бронхоскопов, контаминированных организмами с медикаментозной устойчивостью18,19,20.
В предложенном ниже видеоматериале рассказывается о том, что бронхоскопы представляют собой особый риск перекрестной контаминации от пациента к пациенту.
Финансовые последствия перекрестной контаминации
Как показывает количественное представление данных по итогам систематизированного изучения литературы, общее число контаминированных бронхоскопов составляет 8,7 %*. Эти данные получены на основе изучения 1664 образов из 13 исследований, проведенных в 8 странах мира25-37.
Поскольку у большинства пациентов, контаминированных посредством бронхоскопов, развивается пневмония8,13, в качестве клинического фактора для расчета издержек были использованы именно затраты, связанные с ИВЛ-ассоциированной пневмонией (25 149 долл. США). С учетом 8%-го риска перекрестной контаминации и инфекционного риска, составляющего 20,21 %, издержки, связанные с перекрестной контаминацией, могут быть рассчитаны следующим образом:
0,08 x 0,2021 x 25 149 = 407 долл. США*
* В зависимости от источников, риск контаминации и инфицирования плюс стоимость лечения ИВЛ-ассоциированной пневмонии.
8%-ный риск перекрестной контаминации25-37 умножаем на риск инфицирования (расчетный показатель по данным Ковалевой и др.8) и на стоимость лечения ИВЛ-ассоциированной пневмонии, которая составляет 25 149 долл. США38.
Во время одной из недавних вспышек инфекции, вызванных синегнойной палочкой, затраты системы здравоохранения на постановку диагноза, госпитализацию и лечение шести пострадавших пациентов оценивались в 243 000 или 40 500 долл. США на одного пациента14.

Для однократного применения. Новые возможности.
Вспышки инфекции заставили врачей сомневаться в безопасности бронхоскопии. Эндоскопы, в т. ч. бронхоскопы, входят в список медицинских устройств, наиболее часто ассоциируемых со вспышками внутрибольничных инфекций15, 16.
Риск перекрестного инфицирования мультирезистентными микроорганизмами в ходе выполнения бронхоскопии у постели больного в ОРИТ может быть существенно уменьшен за счет использования стерильных бронхоскопов для однократного применения.
Бронхоскоп для однократного применения aScope 4 Broncho от компании Ambu позволяет свести риск перекрестного заражения к минимуму. Доставая бронхоскоп непосредственно из заводской упаковки, вы можете быть уверены в его стерильности и не опасаться биопленки, оставшейся после недостаточно эффективной автоматической повторной обработки.
Ссылки
CDC Guideline 2008. Disinfection and Sterilization in Healthcare Facilities.
US senate report January 13, 2016 Preventable Tragedies: Superbugs and How Ineffective Monitoring of Medical Device Safety Fails Patients.
Институт ECRI: https://www.ecri.org/Pages/default.aspx
FDA News Release. FDA releases final guidance on reprocessing of reusable medical devices. March 12, 2015.
Reprocessing Medical Devices in Health Care Settings: Validation Methods and Labeling. Guidance for Industry and Food and Drug Administration Staff. FDA. March 17, 2015.
Перейти к статье: Infections Associated with Reprocessed Flexible Bronchoscopes: FDA Safety Communication.
Перейти к: База данных FDA MAUDE.
Kovaleva et al. 2013; Transmission of Infection by Flexible Gastrointestinal Endoscopy and Bronchoscopy. Clinical Microbiology Rev. April 2013 vol. 26 no. 2, p. 231-254.
MM. Mughal et al.2004; Reprocessing the Bronchoscope: The Challenges, Seminars in Respiratory and Critical Care Medicine. Vol. 25 no. 4, p. 443-449.
Pajkos et al. Is biofilm accumulation on endoscope tubing a contributor to the failure of cleaning and decontamination? Journal of Hospital Infection 2004, 58:224-229.
Terjesen et al. 2017; Early Assessment of the Likely Cost Effectiveness of Single-Use Flexible Video Bronchoscopes.
Michelle Alfa Ph.D.; Endoscope Reprocessing Verification Testing, Presentation, Meeting Materials Non-FDA Generated, FDA Committee Meeting, May 14-15, 2015.
R. Douglas Scott II, The Direct Medical Costs of Healthcare-Associated Infections in U.S. Hospitals and the Benefits of Prevention, Division of Healthcare Quality Promotion, National Center for Preparedness, Detection, and Control of Infectious Diseases, Centers for Disease Control and Prevention, March 2009.
Kovaleva et al. Usefulness of Bacteriological Monitoring of Endoscope Reprocessing, Therapeutic Gastrointestinal Endoscopy, Chap. 9, p. 141-162, 2011.
Srinivasan et al. An Outbreak of Pseudomonas aeruginosa Infections Associated with Flexible Bronchoscopes. The New England Journal of Medicine, 2003; 348;221-7.
CDC release from the Healthcare Infection Control Practices Advisory Committee (HICPAC) January 25, 2017. "Essential Elements of a Reprocessing Program for Flexible Endoscopes – Recommendations of the HICPAC”
Cori L. Ofstead et al 2018; Residual moisture and waterborne pathogens inside flexible endoscopes: Evidence from a multisite study of endoscope drying effectiveness.
T. Waite et al 2016; Pseudo-outbreaks of Stenotrophomonas maltophilia on an intensive care unit in England.
Janine Zweigner et al 2014; A carbapenem-resistant Klebsiella pneumoniae outbreak following bronchoscopy.
T Agerton et al 1997; Transmission of a highly drug-resistant strain (strain W1) of Mycobacterium tuberculosis. Community outbreak and nosoco- mial transmission via a contaminated bronchoscope.
Ofstead et al 2017: Longitudinal assessment of reprocessing effectiveness for colonoscopes and gastroscopes: Results of visual inspections, biochemical markers, and microbial cultures.
Kovaleva and Buss: Usefulness of Bacteriological Monitoring of Endoscope Reprocessing.
The Joint Commission: Quick Safety Issue 33 May 2017.
Ofstead et al. 2018 “Effectiveness of reprocessing for flexible bronchoscopes and endobronchial ultrasound bronchoscopes” CHEST.
M. Guy et al. “Outbreak of pulmonary Pseudomonas aeruginosa and Stenotrophomonas maltophilia infections related to contaminated bronchoscope suction valves” Europe's journal of infectious diseases epidemiology, prevention and control Eurosurveillance, Volume 21, Issue 28, 14 July 2016.
C. Ofstead et al 2016 “Practical toolkit for monitoring endoscope reprocessing effectiveness: Identification of viable bacteria on gastroscopes, colonoscopes, and bronchoscopes.”
Cori L. Ofstead et al. 2018 “Residual moisture and waterborne pathogens inside flexible endoscopes: Evidence from a multisite study of endoscope drying effectiveness.”
P. Batailler et al 2015 “Usefulness of Adenosinetriphosphate Bioluminescence Assay (ATPmetry) for Monitoring the Reprocessing of Endoscopes.”
M. Botana-Rial et al 2016 “A Pseudo-Outbreak of Pseudomonas putida and Stenotrophomonas maltophilia in a Bronchoscopy Unit.”
C. DiazGranados et al 2009 “Outbreak of Pseudomonas aeruginosa Infection Associated With Contamination of a Flexible Bronchoscope.”
L. Gavaldà et al 2015 “Microbiological monitoring of flexible bronchoscopes after high-level disinfection and flushing channels with alcohol: Results and costs.”
T. Guimarães et al 2016 “Pseudooutbreak of rapidly growing mycobacteria due to Mycobacterium abscessus subsp bolletii in a digestive and respiratory endoscopy unit caused by the same clone as that of a countrywide outbreak.”
M. Marino et al 2012 “Is Reprocessing After Disuse a Safety Procedure for Bronchoscopy?”
D. Rosengarten et al 2010 “Cluster of Pseudoinfections with Burkholderia cepacia Associated with a Contaminated Washer ‐ Disinfector in a Bronchoscopy Unit.”
N. Shimono et al 2008 “An outbreak of Pseudomonas aeruginosa infections following thoracic surgeries occurring via the contamination of bronchoscopes and an automatic endoscope reprocessor.”
S. Vincenti et al 2014 “Non-fermentative gram-negative bacteria in hospital tap water and water used for haemodialysis and bronchoscope flushing: Prevalence and distribution of antibiotic resistant strains.”
T.D. Waite et al “Pseudo-outbreaks of Stenotrophomonas maltophilia on an intensive care unit in England.”
R. Douglas 2009 “The Direct Medical costs of Healthcare-Associated Infections in U.S. Hospitals and the Benefits of Prevention”

